Sistemas materiales |
Un sistema material está constituido por diferentes cuerpos que forman un todo analizable.
Básicamente, existen dos tipos de sistemas materiales: Homogéneos y Heterogéneos.
Sistemas Homogéneos:
Son aquellos sistemas materiales cuyos componentes poseen las mismas propiedades fisicoquímicas, mostrando una continuidad en toda su masa. No se observan cambios en la estructura de los componentes.
Aquí conviene recordar el concepto de Disolución, como sistema material homogéneo:
Una disolución es una mezcla homogénea que se crea cuando dos o más sustancias se unen entre ellas, estas sustancias no llevan a cabo una reacción. Las disoluciones siempre tienen un componente que disuelve llamado disolvente y un componente que es disuelto llamado soluto.
Sistema homogéneo formado por tres componentes
Ejemplos de disoluciones homogéneas con tres componentes pueden ser:
1) Agua + sal + azúcar (Cuanto la mezcla está insaturada o completamente saturada).
2) Agua + limón + azúcar (Cuando la mezcla está insaturada o completamente saturada).
3) Agua + café + azúcar (Cuando la mezcla está insaturada o completamente saturada).
Otros ejemplos:
Agua solo con sal disuelta: También es homogéneo.
Agua y alcohol Es homogéneo ya que ambos líquidos son miscibles; es decir, se mezclan bien.
Sistema homogéneo formado por un solo componente
Agua pura
Ver: Métodos de separación de mezclas
Sistemas heterogéneos:
Un sistema heterogéneo es aquel que está compuesto por diferentes elementos (de dos o más fases), los cuales pueden diferenciarse a simple vista unos de otros. Es decir que con ellos no se presenta una homogeneidad al tener los componentes diferentes propiedades intensivas (como, por ejemplo, la conocida densidad).
Se le llama fase a cada uno de los sistemas homogéneos dentro de un sistema total (separados de forma definida), lo cual divide al sistema heterogéneo.
Los componentes son aquellas sustancias o materia que forman el sistema total.
Si requieres un ejemplo de un sistema heterogéneo con tres fases y dos componentes, quiere decir que se distinguirán tres zonas diferentes con tan solo dos sustancias diferentes, por ejemplo:
-2 Componentes: agua, y aceite
-3 Fases: agua sólida (hielo), agua en estado líquido y el aceite.
Donde claramente el agua y el aceite son inmiscibles (no se mezclan). Tendremos tres fases ya que los cubos de hielo quedan flotando, el agua líquida en el fondo y el aceite en la parte superior.
Otro ejemplo: Al hervir agua y arroz en un recipiente cerrado.
- 2 Componentes: agua y arroz.
- 3 Fases: agua líquida, vapor de agua y arroz
Sistema heterogéneo con 2 fases y 3 componentes
3 Componentes: Agua-Arena-Sal
2 Fases: agua líquida y arena y sal sólidos
Otros
3 Componentes: Agua-Vinagre- Arroz
2 fases: agua y vinagre líquidos y arroz sólido.
Sistema heterogéneo con 2 fases y 2 componentes
2 componentes: Agua y arena: La arena es depositada en el fondo del recipiente y se diferencia del agua que queda en la parte superior.
2 fases: agua líquida y arena sólida
Como ejercicios, veamos algunos otros ejemplos de sistema heterogéneos:
Agua, aceite y alcohol: En este caso estamos en presencia de un sistema heterogéneo, con dos fases (Aceite por un lado y agua y alcohol por otro) y tres componentes, agua, aceite y alcohol.
Agua y hielo: Tenemos dos fases (agua líquida y hielo) y un solo componente que es el agua.
Bebida gaseosa: Podemos tomar a la bebida en sí como un solo componente y al gas que es el CO2 como el otro. Y dos fases, la líquida y la gaseosa determinada por las burbujas.
Separación de fases:
Existen diferentes métodos para separar fases en los sistemas heterogéneos
Algunas de ellos son:
Decantación:
Este método utiliza como principio la diferencia de densidades entre dos sustancias. Por ejemplo, si queremos separar agua de arena o de otro sólido, vertemos el líquido lentamente desde un recipiente a otro quedando la arena en el fondo.
En el caso de dos líquidos de distintas densidades e inmiscibles, como el agua y el aceite, se usa la ampolla de decantación.
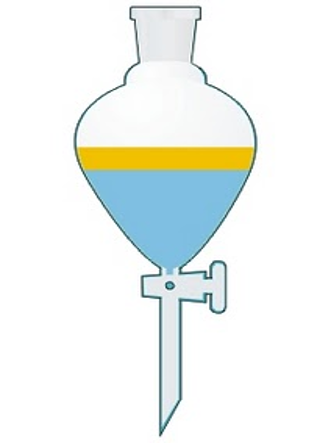
Como se ve en la ilustración, el dispositivo tiene una mariposa en su parte de abajo, la cual permite extraer los líquidos en forma separada.
Filtración:
Es para separar un sólido de un líquido. Especialmente si el sólido consta de partículas pequeñas difíciles de separar por decantación.

Como se ve en la figura, el contenido se vierte por la parte superior y por gravedad el líquido caerá atravesando el filtro intermedio, mientras los sólidos quedarán retenidos en el filtro.
Tamización:
Es una especie de filtración. Pero se usa más para separar sólidos pequeños de sólidos grandes. Generalmente tienen forma de rectángulo de madera con malla metálica en su interior.
Centrifugación:
Este método usa la velocidad de centrifugación para acelerar la separación de las partículas sólidas o semisólidas del líquido. Están equipadas de un motor rotatorio, de una tapa y de unos controles para regular la velocidad y el tiempo de centrifugación.
Lexivigación:
No es ya un método muy utilizado. Antiguamente, era usado para recuperar por arrastre de una corriente de agua las partículas que vayan precipitando y siendo recogidas posteriormente. Fue un método practicado para recolectar piedritas de oro.
Magnetismo:
Es justificado cuando hay presencia de metales en el sistema heterogéneo, como limaduras de hierro.
Fraccionamiento de Fases:
Luego de la separación de fases a veces es necesario separar los componentes que forman dicha fase o el sistema homogéneo que constituye. Esto se denomina métodos de fraccionamiento.
Destilación:
Básicamente hay dos tipos de destilación. La simple y la fraccionada.
Destilación simple: Consiste en la separación de los sólidos de un líquido, que no se pueden separar normalmente por otros métodos. Los sólidos están compuestos de partículas muy pequeñas. El caso más común es cuando tenemos que separar la sal del agua.
Destilación fraccionada: Este tipo de destilación es aplicada para separar líquidos de distinto punto de ebullición. Por ejemplo, agua y alcohol. Se utiliza otro refrigerante.
Cromatografía:
Es un proceso complejo por su variación en cuanto a los distintos tipos de cromatografía. Pero en general podemos decir que consta de dos fases, una móvil y otra estacionaria.
Durante el proceso. los distintos componentes de la mezcla se van separando y así permiten que sean identificados.
Hoy en día hay dispositivos de alta tecnología que acortan los tiempos y lo más importantes son enormemente exactos en la separación.
Cristalización:
Algunas sustancias pueden separarse cuando están en solución formando cristales. Esto depende del tipo de solvente usado y de las temperaturas. Los cristales empiezan a formarse al ir descendiendo la temperatura.

